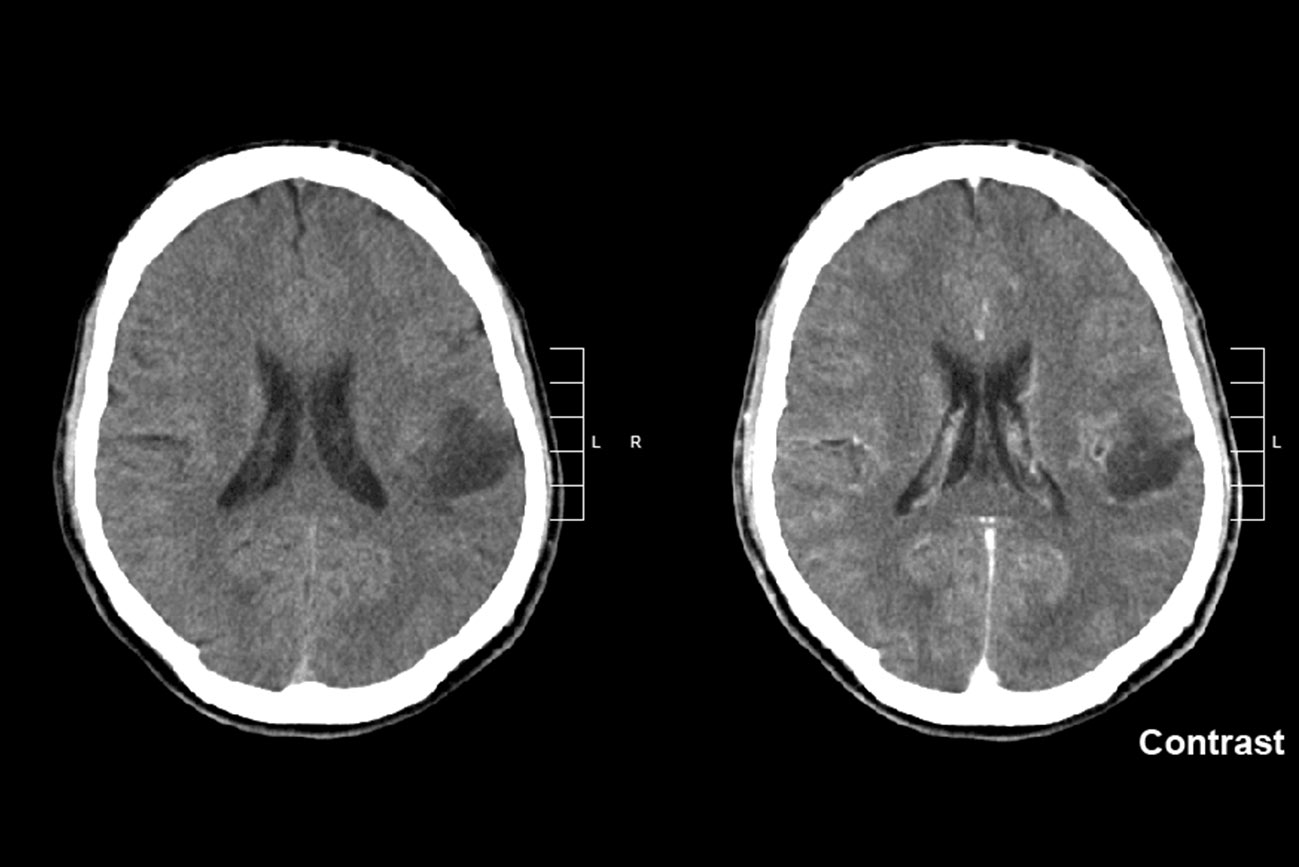
El glioma es un tipo de tumor cerebral que comienza con la multiplicación de las células en el cerebro o la médula espinal. Las células de estos gliomas son muy parecidas a las neuronas cerebrales sanas (células gliales) que rodean las células nerviosas y ayudan a su funcionamiento. No todos los gliomas se consideran cáncer y crecen lentamente. Cuando son malignos, pueden invadir los tejidos sanos y crecer muy rápido. Por otro lado, hay gliomas que afectan a los adultos y otros a los niños.
Un tipo de tumor muy común
Según informa la Clínica Mayo en su web, los gliomas son hasta el 33 por ciento de los tumores cerebrales. Este tipo de tumor es conocido como intra-axial ya que crecen dentgro de la sustancia blanca del cerebro. También se clasifican, según la misma fuente, en astrocitomas, gliomas del tronco encefálico, ependimomas, gliomas mixtos (u oligogastrocitomas), oligodendrogliomas y gliomas del nervio óptico.
En función de la parte del sistema nervioso central en que se encuentren, los síntomas son variados, desde dolor de cabeza y náuseas a convulsiones, pérdida de fuerza o entumecimiento. Otros gliomas, en cambio, no producen ningún síntoma. Para detectarlos se utiliza resonancia magnética y después una biopsia dará el diagnóstico definitivo.
Un fármaco prometedor contra el glioma
Con el nombre técnico de LAM561 (ácido 2-hidroxioleico) Laminar Pharma desarrolla un derivado sintético del ácido oleico que puede ingerirse por vía oral y que podría llegar a las células del cerebro cruzando la barrera hematoencefálica. Como explican en su web “Este fármaco altera la composición de la membrana plasmática de las células cancerígenas, reduciendo la actividad de las proteínas de señalización asociadas a la membrana que se sabe impulsan el crecimiento del tumor. La administración de LAM561 muestra resultados prometedores en el tratamiento de tumores cerebrales agresivos, glioblastomas”.
El fármaco LAM561 y la enfermedad pediátrica rara
Recientemente, la U.S. Food & Drug Administration (FDA) le ha concedido a Laminar Pharma la designación de enfermedad pediátrica rara (RPD) al fármaco LAM561, aún en investigación, orientado a pacientes con glioma difuso de alto grado de tipo pediátrico.
La Dra. Victoria Lladó, directora científica de la filial estadounidense, ‘Laminar Pharma Inc’, asegura que los pacientes pediátricos que lo desarrollan “se enfrentan a unas opciones de tratamiento limitadas y presentan características distintas a las de los pacientes adultos”. Para la doctora, dicha designación como RPD pone sobre la mesa las graves manifestaciones y riesgos que trae consigo la enfermedad para la vida de la población pediátrica que lo padece. Por tanto, afirma que la designación supone un apoyo más de cara a la apuesta de Laminar Pharma por “proporcionar LAM561 como una nueva opción de tratamiento potencial para nuestros pacientes”.
Los pacientes pediátricos que lo desarrollan “se enfrentan a unas opciones de tratamiento limitadas y presentan características distintas a las de los pacientes adultos”.
Buscando tratamientos para las enfermedades pediátricas raras
El objetivo del programa RPD no es otro que el de promover el desarrollo de nuevos fármacos para el tratamiento de enfermedades pediátricas raras. Tanto es así, que la designación se otorga por medio de la FDA a aquellas enfermedades que conlleven un riesgo para la vida, que afectan a menos de 200.000 personas en Estados Unidos y en las que las manifestaciones graves tienen lugar principalmente en una franja de edad inferior a los 18 años.
En este escenario, Laminar Pharma podría ser elegible para optar a una revisión prioritaria en cualquier solicitud de marketing posterior si, en el futuro, la FDA aprueba una solicitud de nuevo medicamento para el fármaco que desarrolla la compañía. Un fármaco que, tiempo atrás, la FDA y la Agencia Europea de Medicamentos ya otorgaron la nomenclatura de producto medicinal huérfano para el tratamiento del glioma maligno, o la designación Fast-Track en 2022 para tratar el glioblastoma.

Equipo de Laminar Pharma
El desarrollo clínico de LAM561 incluye dos estudios completados con éxito para determinar su seguridad y tolerabilidad en pacientes adultos. Uno de ellos en pacientes con tumores sólidos avanzados y otro en pacientes recién diagnosticados en combinación con el tratamiento estándar. Además, cuentan con otros dos ensayos clínicos que, actualmente, se están llevando a cabo. Uno para el tratamiento de pacientes adultos recién diagnosticados y en combinación con la atención estándar europea; y otro cuya meta es averiguar la seguridad, tolerabilidad y potencial actividad clínica en aquellos pacientes pediátricos con tumores sólidos avanzados en Estados Unidos.
Esta es una información elaborada a partir de un comunicado de Laminar Pharma, la Universidad Johns Hopkins y la Clínica Mayo. Por favor, consulte siempre a su médico.
Glioma en el lóbulo parietal izquierdo.
Imagen: Mikhail Kalinin Mikhail Kalinin, CC BY-SA 3.0 <https://creativecommons.org/licenses/by-sa/3.0>, via Wikimedia Commons